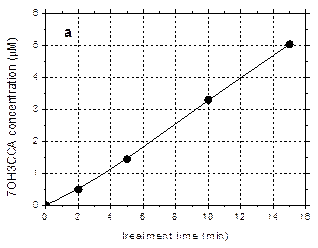Raport stiintific
privind implementarea proiectului „Mecanisme de degradare a poluantilor organici persistenti din apa cu plasma netermica si sisteme combinate plasma-ozonizare”, contract nr. 71 / 2017, in perioada iulie – decembrie 2017
Scopul proiectului consta in studiul mecanismelor de degradare a poluantilor din apa in plasma netermica si cu plasma combinata cu ozonizare (cu ozon generat in plasma). Cercetarile se indeapta spre poluanti organici persistenti (POP), caracterizati de stabilitate ridicata si rezistenti la procesele de degradare obisnuite. Multi dintre acesti compusi prezinta un grad inalt de toxicitate si pot afecta negativ organismele acvatice si nu numai. Se urmareste investigarea proceselor ce au loc in descarcari electrice in contact cu apa, procese ce conduc la formarea de specii oxidante, precum si a reactiilor chimice intre acesti oxidanti si compusii organici tinta. Etapa actuala a proiectului are ca obiectiv cuantificarea celor mai importante specii oxidante generate in plasma, pe de o parte pentru identificarea conditiilor experimentale care maximizeaza concentratiile acestor oxidanti si pe alta parte in vederea ajustarii concentratiilor oxidantilor prin varierea parametrilor descarcarii electrice. Un alt obiectiv consta in efectuarea unor teste de degradare in plasma: determinarea ratei de descompunere, gradului de mineralizare, identificarea unor produsi de degradare, evaluarea eficientei energetice.
Dispozitiv experimental
Experimentele au fost realizate intr-o descarcare corona pulsata generata in gaz deasupra lichidului [1] (Fig. 1). Reactorul de plasma de forma paralelipipedica (8.5 cm x 16 cm) contine un electrod de masa plasat pe suprafata inferioara si un electrod de inalta tensiune constand intr-o retea de fire subtiri si pozitionat la ~9 mm deasupra electrodului de masa. Reteaua de fire consta in 20 fire de cupru (diametru 100 mm, lungime 36 mm) paralele, plasate la 6 mm unul fata de celalalt. Solutia din vas are o adancime de aproximativ 5 mm.
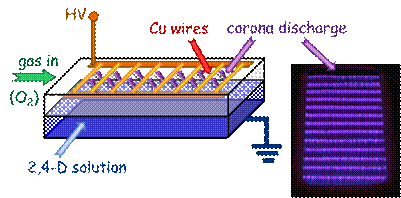
Fig. 1. Schema reactorului de plasma si fotografia descarcarii corona
Descarcarea corona este de natura filamentara (vezi fotografie Fig. 1), filamentele pornesc de la fire si se propaga spre suprafata apei, deci plasma este generata in gaz si este in contact cu lichidul.
In general, in experimente s-a folosit apa de robinet (conductivitate ~370 mS/cm, pH 7.5) si nu apa distilata, pentru a fi mai aproape de o situatie reala de tratare a apei. Ca gaz de lucru a fost utilizat oxigen, introdus prin reactorul de plasma cu debitul de 300 mL/min. Concentratia de O3 din gaz a fost masurata cu un detector comercial (Ozomat MP, Anseros). Pentru detectia ozonului din faza lichida s-a folosit o metoda colorimetrica, bazata pe decolorarea unei solutii de indigo trisulfonat [2]. Concentratia de H2O2 din lichid a fost determinata de asemenea printr-o metoda spectrofotometrica ce utilizeaza reactia sulfatului de titan cu H2O2 [3]. Formarea radicalilor hidroxil (•OH) in solutiile tratate cu plasma a fost evaluata prin monitorizarea conversiei acidului coumarin 3-carboxilic (3CCA) intr-un compus fluorescent (acid 7-hidroxi-3-carboxilic, 7OH3CCA) prin reactia cu •OH [4,5].
Compusul tinta investigat in experimentele de degradarea in plasma a fost pesticidul 2,4-D (acid 2,4-diclorofenoxiacetic) cu o concentratie initiala de 25 mg/L. Analiza solutiilor apoase s-a efectuat prin cromatografie de lichid (HPLC) pentru determinarea ratei de degradare si gradului de declorinare si prin analiza de carbon organic total (TOC) pentru determinarea gradului de mineralizare.
Rezultate
Caracteristicile electrice ale descarcarii
Pulsurile de inalta tensiune au fost produse prin doua metode: (1) prin descarcarea unui condensator (6 nF, 4 nF sau 2 nF) folosind un comutator cu tiristor (Behlke HTS 240-800-SCR) – Fig. 2a; (2) cu ajutorul unei linii de formare bazata pe un cablu coaxial (lungime 10 m sau 6.5 m) folosind un comutator cu autostrapungere – Fig. 2b, iar caracteristicile principale sunt prezentate in Tabelul 1.
Tensiunea de descarcare a fost masurata cu o sonda Tektronix P6015, iar curentul cu o sonde Tektronix TCP0150 si au fost monitorizate cu ajutorul unui osciloscop Tektronix DPO 2024. In toate experimentele s-a folosit polaritate negativa a tensiunii, amplitudinea pulsurilor de tensiune a fost mentinuta constanta la aproximativ 18 kV, iar frecventa pulsurilor a fost fixata la 25 Hz.
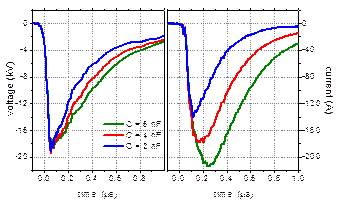
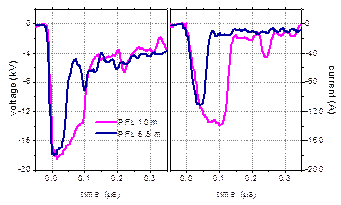
Fig. 2. Pulsurile de tensiune si curent de descarcare obtinute prin cele doua metode: (a) condensatori de 6, 4 si 2 nF; (b) linie de formare cu cablu de 10 m si 6.5 m.
Timpul de crestere a tensiunii (tr) este dictat de comutator si are o valoare de aproximativ 27 ns (masurat de la 10 la 90% din amplitudine). Cum era de asteptat, scaderea capacitatii condensatorului conduce la reducerea duratei pulsurilor de tensiune (Fig. 2a). Astfel, pentru condensatorul de 6 nF (notatie C6nF in Tabelul 1 si in figurile ulterioare) durata pulsurilor este de 430 ns (masurata la 50% din amplitudine), in timp ce pentru capacitatea de 2 nF (C2nF) au fost obtinute pulsurilor de largime 250 ns. O comportare asemanatoare este vizibila si pentru pulsurile de curent. In acelasi timp, se observa o diminuare considerabila a amplitudinii pulsurilor de curent odata cu scaderea capacitatii condensatorului: de la 214 A pentru condensatorul de 6 nF pana la 140 A obtinuti cu 2 nF.
Pentru pulsurile obtinute cu linia de formare, timpul de crestere este mult mai scurt decat al celor produse cu condensator, de numai 11-12 ns. Durata pulsurilor este in acest caz determinata de lungimea cablului coaxial, fiind egala cu dublul timpului necesar pentru propagarea pulsului de-a lungul cablului. Astfel, pentru cablul de 10 m lungime (notat cu PFL10m in Tabelul 1 si in figurile urmatoare), largimea pulsului este de 108 ns, iar pentru cablul mai scurt (PFL6.5m) au fost obtinute pulsuri de 54 ns. Amplitudinea curentului pentru PFL10m este similara cu cea obtinuta cu condensatorul de 2 nF (138 A) si scade pentru pulsurile mai scurte (PFL6.5m).
Energia pe puls (Ep) si puterea medie disipata in descarcare (P) au fost calculate conform ecuatiilor:
![]()
![]()
unde t1 and t2 reprezinta inceputul si sfarsitul pulsului, I este curentul, V este tensiunea, iar n este rata de repetitie a pulsurilor, care a fost constanta (25 Hz) in toate experimentele.
Tabelul 1. Caracteristicile pulsurilor de tensiune si curent ale descarcarii corona (tr – timpul de crestere pentru pulsurile de tensiune (10-90%), tv, tI – durata pulsurilor de tensiune, respectiv curent (FWHM), Imax – amplitudinea pulsurilor de curent, Ep – energia pe puls, P – puterea medie disipata in descarcare)
|
experiment |
tr (ns) |
tV (ns) |
tI (ns) |
Imax (A) |
Ep (J) |
P (W) |
|
C6nF |
29 |
430 |
470 |
214 |
1.24 |
31 |
|
C4nF |
27 |
340 |
360 |
176 |
0.86 |
21.6 |
|
C2nF |
27 |
250 |
230 |
140 |
0.46 |
11.4 |
|
PFL10m |
11 |
108 |
103 |
138 |
0.20 |
5 |
|
PFL6.5m |
12 |
54 |
47 |
110 |
0.08 |
2.1 |
Asa cum se vede in Tabelul 1, energia pe puls si puterea medie de descarcare pot fi variate intr-un domeniu destul de larg prin modificarea duratei de puls. Astfel, puterea scade de la 31 W pentru cele mai lungi pulsuri (C6nF) pana la 2.1 W pentru pulsurile cele mai scurte (PFL6m).
Detectia speciilor oxidante generate in plasma
Cele mai importante specii oxidante formate in plasma in apa sau in contact cu apa, relevante din punct de vedere al reactiilor chimice cu moleculele de poluant din lichid, sunt ozonul (O3), radicalii hidroxil (•OH) si peroxidul de hidrogen (H2O2).
Ozonul este un oxidant puternic (potential redox Eo = 2.07 V) a carui formare in plasma este binecunoscuta. Generarea O3 in plasma este initiata de disocierea oxigenului molecular prin ciocnire electronica (R1), urmata de reactia oxigenului atomic cu O2 (R2):
e- + O2 à O + O (R1)
O + O2 + M à O3 + M (R2)
Desi O3 se formeaza in faza gazoasa, atunci cand descarcarea este generata in proximitatea suprafetei lichidului, ozonul poate fi transferat din gaz in lichid si astfel poate contribui la oxidarea compusilor organici poluanti din solutie. Oxidarea cu ozon poate avea loc atat prin reactii directe, cat si indirect, prin radicali OH formati la descompunerea O3 (R3). Totusi reactia directa este relativ lenta comparativ cu oxidarea prin radicali OH, deoarece O3 este foarte selectiv si dependent de pH.
O3 + H2O à OH + O2 + HO2 (R3)
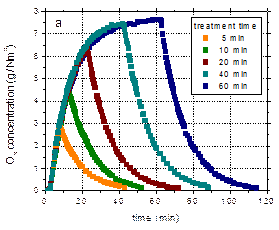
Variatia temporala a concentratiei de ozon din gaz este prezentata in Fig. 3a pentru experimentele efectuate cu apa, in cazul pulsurilor scurte de tensiune (54 ns) obtinute cu linia de formare de 6.5 m (PFL6.5m). A fost variata durata experimentului in domeniul 5-60 min, iar pentru fiecare experiment apa din reactorul de plasma a fost schimbata. Concentratia maxima de O3 atinsa dupa 60 min de tratare in plasma este de ~7.6 g/Nm3 (Fig. 3a). Cantitatea totala de O3 produs in plasma a fost calculata prin integrarea concentratiei pe durata experimentului. A fost studiat efectul duratei pulsului de tensiune asupra cantitatii de O3 formate. In Fig. 3b sunt ilustrate aceste rezultate in functie de timpul de expunere la plasma, iar in Fig. 3c in functie de energia introdusa in descarcare, pentru diferite largimi de puls in domeniul investigat (54 – 430 ns). Fig. 3d prezinta eficienta de generare a O3.
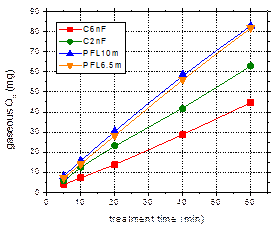
Se observa variatia liniara a cantitatii de O3 din gaz cu timpul de operare a plasmei, pentru toate largimile de puls investigate. Reducerea duratei pulsului are un efect pozitiv asupra generarii de ozon in plasma (Fig. 3b): astfel, pentru pulsurile lungi (430 ns) obtinute cu ajutorul condensatorului de 6 nF cantitatea de O3 produsa in plasma in timp de 60 min a fost de ~45 mg, ea creste la 63 mg pentru pulsurile de 250 ns (condensator de 2 nF) si atinge 82-83 mg pentru pulsurile de 108 si 54 ns obtinute cu liniile de formare (PFL10m si PFL6.5m). Tendinta observata in Fig. 3b sugereaza ca o reducere a duratei de puls sub 50 ns ar conduce la scaderea concentratiei de O3, deci maximul concentratiei este atins pentru pulsuri de 50-100 ns.
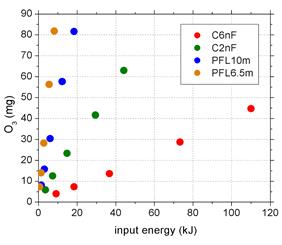
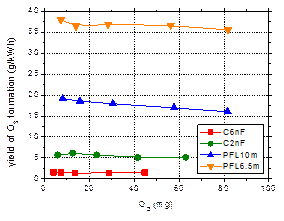
Fig. 3c prezinta aceste rezultate in functie de energia introdusa in descarcare. Inputul energetic este un parametru mult mai util, deoarece combina timpul de tratare si puterea medie disipata in descarcare, care difera pentru diferite durate de puls (E = P × t). Graficul evidentiaza foarte clar avantajul pulsurilor scurte in producerea ozonului: aceeasi cantitate de O3 poate fi generata cu un input energetic mult mai mic reducand largimea pulsului, ceea ce denota o eficienta mult superioara. Intr-adevar, Fig. 3d arata ca eficienta de producere a ozonului in descarcarea corona operata cu pulsuri scurte (PFL6.5m) este cu mai mult de un ordin de marime superioara celei obtinute cu pulsuri lungi (C6nF). Acest rezultat sugereaza ca o parte importanta din puterea disipata in descarcare in cazul pulsurilor lungi este practic pierduta prin efect Joule, fiind consumata pentru incalzirea gazului si lichidului. Este cunoscut faptul ca temperatura ridicata are un efect negativ asupra producerii O3, rata de descompunere a acestuia fiind puternic dependenta de temperatura. Eficienta cea mai ridicata (~36 g/kWh) a fost atinsa pentru pulsurile cele mai scurte (54 ns – PFL6.5m), insa cantitatea de O3 formata in acest caz este similara, sau chiar usor mai mica decat cea produsa cu pulsurile de 108 ns (PFL10m).
|
|
|
|
|
|
|
Fig. 3. a – Concentratia de ozon in functie de timp pentru experimente cu pulsuri de 54 ns (PFL6.5m); b – Cantitatea totala de O3 produs in plasma pentru diferite durate de puls in domeniul 54-430 ns; c – Cantitatea de O3 in functie de energia introdusa in descarcare; d – Eficienta de formare a O3 in plasma pentru diferite durate de puls in domeniul 54-430 ns |
|
Radicalul hidroxil este cea mai importanta specie chimica generata in descarcari electrice in apa sau in contact cu lichid. Este un oxidant foarte puternic (Eo = 2.85 V) si reactioneaza neselectiv cu majoritatea compusilor organici si multi compusi inorganici. In plasma, radicalii •OH se produc in principal prin disocierea moleculelor de apa prin ciocniri electronice (R4):
e- + H2O à •OH + •H (R4)
Formarea radicalilor •OH in solutiile tratate cu plasma a fost evidentiata prin monitorizarea producerii de 7OH3CCA prin reactia intre 3CCA si •OH (Fig. 4). In principiu, concentratia de •OH este proportionala cu concentratia de 7OH3CCA format, presupunand ca acest compus nu este la randul lui descompus pe parcursul experimentului. Pentru a evita distrugerea 7OH3CCA de catre ozon, timpul de expunere la plasma a fost limitat la 15 min, iar degradarea 3CCA a fost de asemenea urmarita si corelata cu formarea 7OH3CCA.
Concentratia de 7OH3CCA prezinta o dependenta liniara de timpul de tratare in plasma si atinge 5 mM dupa 15 min (Fig. 4). S-a observat ca liniaritatea nu se pastreaza pentru durate de tratare mai lungi datorita cresterii conversiei compusului parinte (3CCA) si interferentei produsilor de reactie. In literatura a fost raportata o valoare de 4.7% pentru eficienta de formare a 7OH3CCA pe radical •OH [5]. In consecinta, rata de formare de radicali •OH in apa expusa la plasma corona operata cu pulsuri lungi (430 ns) poate fi estimata la 4x10-2 mmol/s.
|
Fig. 4. Concentratia de 7OH3CCA format intr-o solutie 1 mM de 3CCA expusa la plasma (tV = 430 ns – C6nF); |
Peroxidul de hidrogen este o alta specie activa importanta produsa in plasma in lichid si sisteme gaz-lichid. Se formeaza in principal prin disocierea moleculei de apa prin ciocniri electronice (R4), urmata de recombinarea radicalilor •OH (R5).
•OH + •OH à H2O2 (R5)
H2O2 este caracterizat de o solubilitate ridicata in apa si timp de viata lung, precum si un potential de oxidare relativ ridicat (Eo = 1.77 V). Ca si ozonul, H2O2 poate reactiona cu compusii organici atat direct, cat si indirect. Desi ratele de reactie directa sunt in general mici, H2O2 este important pentru tratarea apei datorita reactiilor indirecte, cu formare de radicali •OH: reactia Fenton in prezenta catalizatorilor de fier (R6), reactia cu ozon (R7) si fotoliza UV (R8).
Fe2+ + H2O2 à Fe3+ + •OH + OH− (R6)
H2O2 + O3 à O2 + •OH + HO2 (R7)
H2O2 + hn à •OH + •OH (R8)
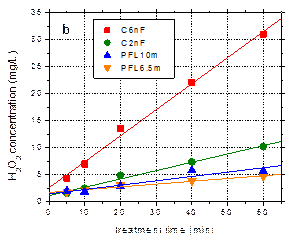
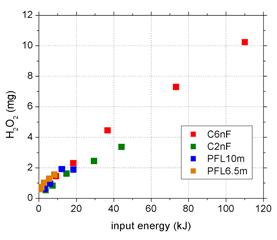
Concentratia de H2O2 format in solutia tratata cu plasma este prezentata in Fig. 4a in functie de timpul de tratare, pentru diferite durate ale pulsurilor de tensiune, in domeniul 54-430 ns. Aceste rezultate sunt ilustrate in Fig. 4b in functie de energia introdusa in descarcare.
|
|
|
|
Fig. 5. a – Concentratia de H2O2 format in apa in functie de timpul de tratare, pentru diferite largimi de puls in domeniul 54-430 ns; b – Cantitatea de H2O2 produs in functie de energia introdusa in descarcare. |
|
Concentratia de H2O2 generat in apa expusa la plasma variaza liniar cu timpul de tratare (Fig. 5a). In cazul pulsurilor lungi (430 ns) a fost detectat semnificativ mai mult H2O2 (peste 30 mg/L in timp de 60 min) fata de pulsurile mai scurte. Responsabila pentru acest rezultat poate fi puterea superioara si, implicit, concentratia mai mare de vapori de apa din gaz, care conduce la o concentratie mai mare de radicali •OH. O alta explicatie a acestui comportament ar putea fi distrugerea H2O2 in reactia cu O3, a carui concentratie creste odata cu reducerea duratei pulsului. Totusi, reprezentarea rezultatelor in functie de energia introdusa in descarcare (Fig. 5b) arata ca diferentele de concentratie nu sunt foarte mari intre diverse largimi de puls.
Degradarea unor poluanti organici cu plasma
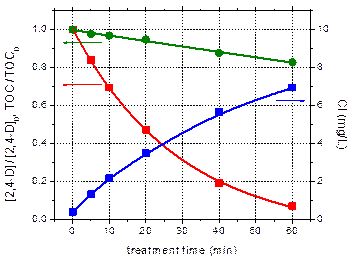
Unul dintre compusii chimici testati in acest studiu este acidul 2,4-diclorofenoxiacetic (2,4-D), un erbicid folosit frecvent pentru distrugerea buruienilor in special la grau si porumb si adesea detectat in apa. Rezultatele obtinute privind degradarea acestui compus in plasma sunt ilustrate in Fig. 6.
|
|
Fig. 6. Variatia concentratiei relative de 2,4-D din solutie (<), a carbonului organic total (=) si a ionilor de clor rezultati in urma descompunerii 2,4-D (p), in functie de timpul de tratare in plasma |
Analiza 2,4-D din solutiile apoase s-a facut prin cromatografie de lichid (HPLC), folosind un aparat VarianProStar cu detector UV-DAD at l = 284 nm si 210 nm si coloana Zorbax SB-C18 (4.6 mm × 250). Faza mobila a fost un amestec de solutie tampon fosfat (20 mM)/acetonitril, 50/50, cu debitul de 1.0 mL/min.
Concentratia de 2,4-D din solutie scade cu timpul de tratare in plasma, dupa o cinetica de ordinul I, iar dupa 60 min de tratare peste 90% din cantitatea initiala de compus este degradata. Eficienta de degradare este definita ca fiind cantitatea de poluant distrusa pe unitate de energie consumata in proces:
![]()
unde c0 este concentratia initiala de 2,4-D din solutie (25 mg/L), Vs este volumul solutiei (0.33 L), R2,4‑D este rata de degradare si Ein este energia introdusa in descarcare.
Valoarea eficientei de descompunere a 2,4-D calculata la 50% degradare este de 450 mg/kWh, iar la 90% de 283 mg/kWh.
Mineralizarea este de asemenea un parametru foarte important, ce reflecta oxidarea totala a compusului la CO2, H2O si alti compusi inorganici. Gradul de mineralizare a 2,4-D a fost evaluat prin analiza de carbon organic total (TOC), folosind un analizor HiPerTOC Thermo Electron, bazat pe absorbtia CO2 in IR. In experimentele de degradare in plasma gradul de mineralizare a fost de aproape 20% dupa 60 min de tratare.
Eliberarea ionilor de clor din molecula de 2,4-D pe parcursul procesului de degradare a fost de asemenea cuantificata prin HPLC, folosing un cromatograf Varian ProStar cu detector de conductivitate si o coloana Dionex IonPac AS22-Fast (4 × 150 mm). Ca faza mobila s-a folosit o solution de carbonat de sodiu si carbonat acid de sodiu (20 mM) cu debitul de 1,2 mL/min. Cantitatea stoichiometrica de Cl- ce se poate obtine din degradarea concentratiei de 2,4-D este de ~8 mg/L. Analiza cantitativa a ionilor Cl- din solutie sugereaza ca produsii de reactie clorinati proveniti din descompunerea 2,4-D sunt de asemenea degradati (in cea mai mare parte) pe parcursul experimentului. In primele minute de tratare s-a observat formarea de 2,4-diclorofenol, care insa dispare rapid, iar la finalul experimentului singurii produsi de reactie detectati sunt cativa acizi carboxilici.
Diseminarea rezultatelor
Rezultatele obtinute in aceasta etapa a proiectului urmeaza a fi valorificate astfel: un articol a fost trimis spre publicare in revista Plasma Processes and Polymers (in evaluare) si sunt in pregatire doua comunicari la conferinte internationale (ISNTP si GD2018) ce vor avea loc in 2018.
Referinte:
[1] D. Dobrin, C. Bradu, M. Magureanu, N.B. Mandache, V.I. Parvulescu, Chem. Eng. J. 234 (2013) 389.
[2] H. Bader, J. Hoigne, Water Res. 15 (1981) 449.
[3] G.M. Eisenberg, Ind. Eng. Chem. Anal. Ed. 15 (1943) 327.
[4] E. Marotta, M. Schiorlin, X. Ren, M. Rea, C. Paradisi, Plasma Process. Polym. 8 (2011) 867.
[5] G.L. Newton, J.R. Milligan, Radiat. Phys. Chem. 75 (2006) 473.
Director proiect,
Dr. Monica Magureanu